第一次!CRISPR基因编辑在活体动物内成功医治癌症,且永久有效

简介:这是世界上首个证明CRISPR基因组编辑系统可用于有效医治活体动物癌症的研究。
【红叶网探索分享】
近年来,分子靶向抑制剂和免疫疗法极大地改善了癌症医治,同时也降低了医治毒性和不良反应。但目前多数抗癌药物都需要重复给药,不仅增加了医治相关的毒性和成本,而且严重降低了患者的生活质量。此外,大多数类型的癌症具有高复发率和耐药性,因此急需开发新的医治方法。
CRISPR-Cas9基因编辑具有永久破坏肿瘤存活基因的潜力,可以克服传统癌症疗法的重复剂量限制,提高医治效果。但Cas9和sgRNA的体积较大,对常规病毒和非病毒递送系统来说具有一定障碍,且当前用于非肝脏组织和肿瘤的递送系统所导致的基因编辑率相对较低。因此,需要实质上更高的编辑效率的新型递送系统来提高癌症医治的有效性。
近日,来自以色列特拉维夫大学的研究人员在《Science Advances》上发表了题为CRISPR-Cas9 genome editing using targeted lipid nanoparticles for cancer therapy的研究成果,其开发了一种新型的基于脂质纳米颗粒的递送系统,使用该系统进行CRISPR-Cas9基因组编辑的效率可达84%以上,且能明显抑制肿瘤的生长,使存活率提高80%。这一创新为癌症医治和研究开辟了新途径,并为非癌组织的靶向基因编辑提供了潜在的应用。

DOI: 10.1126/sciadv.abc9450
脂质纳米颗粒(LNP)是临床认可的非病毒核酸传输系统。研究人员使用Cas9 mRNA替代质粒DNA,并对其和sgRNA进行修饰,以增强RNA稳定性并降低免疫原性,同时设计使用了4个来自新型可电离氨基脂质库的可电离阳离子脂质共封装Cas9mRNA和sgRNA。其中L8-cLNPs(CRISPR LNP)的物种物理性质与临床批准的LNP制剂MC3-cLNPs相似,且Cas9 mRNA和sgRNA的包封效率相比较高。对L8-cLNP破坏基因的效率和特异性进行评估,发现其基因修饰率可达94%,且在非靶向基因座上的编辑率低于0.1%。
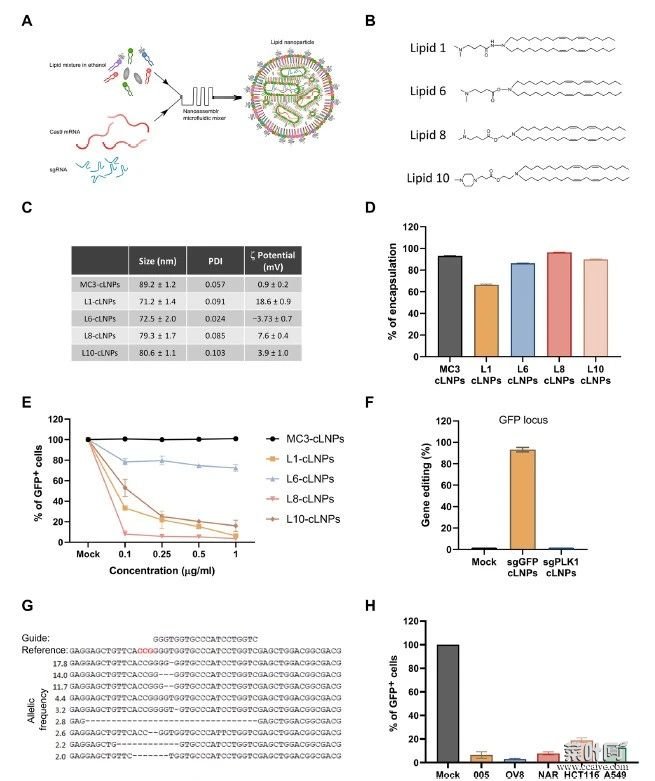
CRISPR LNP(cLNPs)的设计和构建
PLK1是有丝分裂所需的激酶,缺乏它会导致G2-M期细胞周期停滞且分裂细胞死亡。为了探索cLNPs在癌症中进行基因组编辑的潜力,研究人员使用sgPLK1-cLNPs处理了两种侵袭性和难医治的癌症的癌细胞系:胶质母细胞瘤和转移性卵巢癌。结果发现该基因编辑可有效地破坏PLK1基因,在两种癌细胞中编辑率可达84%和91%,处理48小时后两种癌细胞系均出现了细胞周期停滞和死亡,并且经医治相关剂量全身给药实验确保了L8-cLNPs不存在毒性或免疫原性。
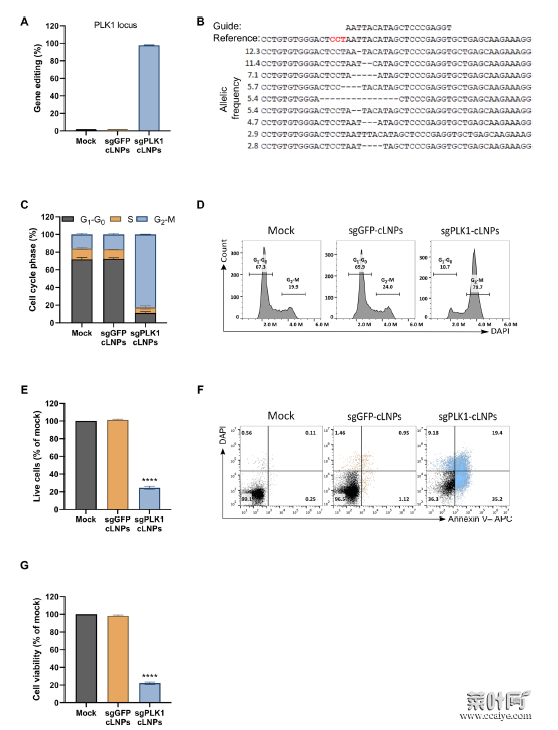
体外HEK293细胞中的医治性基因组编辑
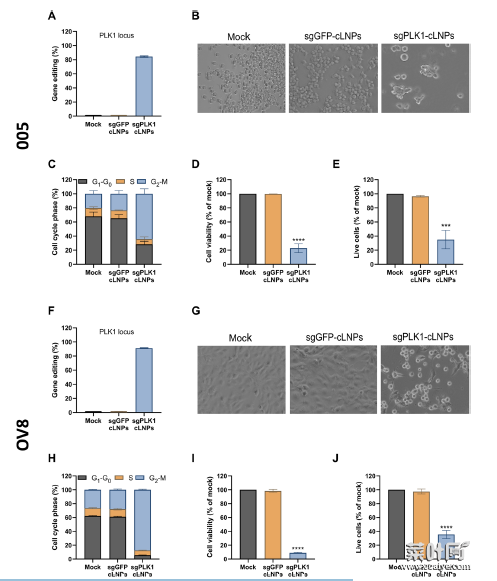
体外胶质母细胞瘤和转移性卵巢癌细胞的医治基因组编辑
然后,研究人员对该cLNPs在体内的医治功效进行了评估。将sgPLK1-cLNPs立体定向注射到已构建的肿瘤小鼠模型中,分析其单细胞肿瘤悬液中的PLK1基因编辑效率及PLK1基因破坏引起的体内细胞凋亡及肿瘤生长抑制情况。肿瘤细胞PLK1基因座中约68%都得到了编辑,且出现了PLK1依赖性细胞凋亡,单次肿瘤内注射sgPLK1-cLNPs也显著抑制了肿瘤的生长,使小鼠的中位生存期从32.5天增加到超过48天,生存率提高了30%。
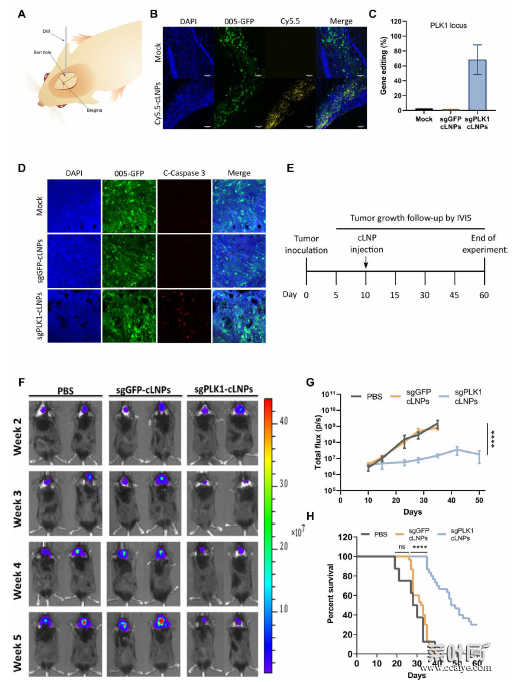
胶质母细胞瘤小鼠的医治性基因组编辑
包括转移性或血液肿瘤在内的多数肿瘤的医治均需要全身给药,但大多数LNP会被困在肝脏和其他中央器官,无法被肿瘤细胞有效吸收。研究人员对靶向EGFR的sgPLK1-cLNPs在转移性卵巢腺癌模型中的疗效进行检测,发现其可有效抑制肿瘤生长并提高总生存率,肿瘤细胞PLK1基因座中约有82%被编辑,小鼠的总生存期提高了约80%。这也说明,靶向性cLNPs可用于靶向医治弥漫性肿瘤。
该研究的通讯作者Dan Peer表示:“这是世界上首个证明CRISPR基因组编辑系统可用于有效医治活体动物癌症的研究。而且这不是化学疗法,没有副作用,用这种方法医治的癌细胞将永远不会再活跃。该技术也为医治其他类型的癌症以及罕见的遗传性疾病和艾滋病等慢性病毒性疾病开辟了许多新的可能性。”
参考资料:
[1] CRISPR-Cas9 genome editing using targeted lipid nanoparticles for cancer therapy
声明:本文内容仅代表作者个人观点,与本站立场无关。如有内容侵犯您的合法权益,请及时与我们联系,我们将第一时间安排处理。更多精彩内容请关注红叶网
-

-

-

-
-

-

-
-
-

-
 大学生买什么笔记本电脑好 前沿科技0人阅读
大学生买什么笔记本电脑好 前沿科技0人阅读 -
-

-
-
 麝香是什么动物身上的哪个部位,雄麝的腺囊的分泌物 前沿科技110人阅读
麝香是什么动物身上的哪个部位,雄麝的腺囊的分泌物 前沿科技110人阅读 -
 石楠花为何叫最污花,因其花香特别像男子的精液一样 前沿科技102人阅读
石楠花为何叫最污花,因其花香特别像男子的精液一样 前沿科技102人阅读 -

-

-
-

-
-

-
 前苏联科学家成功让断开的狗头张嘴复活数小时 前沿科技101人阅读
前苏联科学家成功让断开的狗头张嘴复活数小时 前沿科技101人阅读 -
 暗物质实验发出的信号可能预示着新的物理学原理 前沿科技100人阅读
暗物质实验发出的信号可能预示着新的物理学原理 前沿科技100人阅读 -

-

-
 SpaceX的龙飞船长什么样? 前沿科技100人阅读
SpaceX的龙飞船长什么样? 前沿科技100人阅读